El atomo
Grupo de quimica
Tema: El atomo
Integrantes:
Maria Torres
Nelson Peñafiel
Camila Zambrano
Kelvin Paredes
Bruno Hinojosa
Lisette Sando
Mayte Gordillo
El átomo ¿Qué es?
¿Qué es un átomo? Imagínate que tienes un pedazo de hierro. Lo
partes. Sigues teniendo dos trozos de hierro pero más pequeños. Los
vuelves a partir, otra vez... Cada vez tendrás trozos más pequeños hasta
que llegará un momento, en que si los volvieses a partir lo que te
quedaría ya no sería hierro.
Llegados a este punto lo que ha quedado és un átomo, un átomo de hierro.
Definición de átomo
De un modo más formal, definimos átomo como la partícula más pequeña
en que un elemento puede ser dividido sin perder sus propiedades
químicas.
El origen de la palabra átomo proviene del griego, que significa
indivisible. En el momento que se bautizaron estas partículas se creía
que efectivamente no se podían dividir, aunque hoy en dia sabemos que
los átomos están formados por partículas aún más pequeñas, repartidas en
las dos partes del àtomo, las llamadas partículas subatómicas.
Partes y estructura de un átomo
La estructura de un átomo resulta muy sencilla la cual la dividimos en dos partes: núcleo y corteza.
El núcleo es la parte central de la estructura del átomo. En la parte del núcleo se encuentran los protones (partículas con carga positiva) y los neutrones (partículas sin carga eléctrica).
En la corteza, la parte exterior del átomo se encuentran los electrones (partículas con carga eléctrica negativa).
Los protones, neutrones y electrones
son las partículas subatómicas que forman la estructura del átomo. Lo
que diferencia a un átomo de otro es la relación que se establecen entre
ellas.
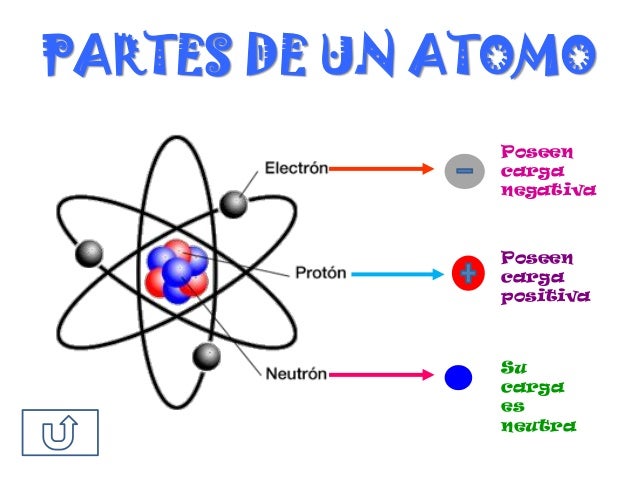 Los electrones, de carga negativa, son las partículas subatómicas más
ligeras. Los protones, de carga positiva, pesan unas 1.836 veces más
que los electrones. Los neutrones, los únicos que no tienen carga eléctrica, pesan aproximadamente lo mismo que los protones.
Los electrones, de carga negativa, son las partículas subatómicas más
ligeras. Los protones, de carga positiva, pesan unas 1.836 veces más
que los electrones. Los neutrones, los únicos que no tienen carga eléctrica, pesan aproximadamente lo mismo que los protones.
Los protones y neutrones se encuentran agrupados en la parte central del átomo formado el núcleo atómico. Por este motivo también se les llama nucleones.
De modo, la parte central del átomo, el núcleo atómico, tiene
una carga positiva en la que se concentra casi toda su masa, mientras
que en el escorzo alrededor del núcleo atómico hay un cierto número de
electrones, cargados negativamente. La carga total del núcleo atómico (positiva) es igual a la carga negativa de los
electrones, de modo que la carga eléctrica total del átomo sea neutra.
Propiedades de los átomos
Las
unidades básicas de la química son los átomos. Durante las reacciones
químicas los átomos se conservan como tales, no se crean ni se
destruyen, pero se organizan de manera diferente creando enlaces
diferentes entre un átomo y otro.
Los átomos se agrupan formando moléculas y otros tipos de materiales. Cada tipo de molécula es la combinación de un cierto número de átomos enlazados entre ellos de una manera específica.
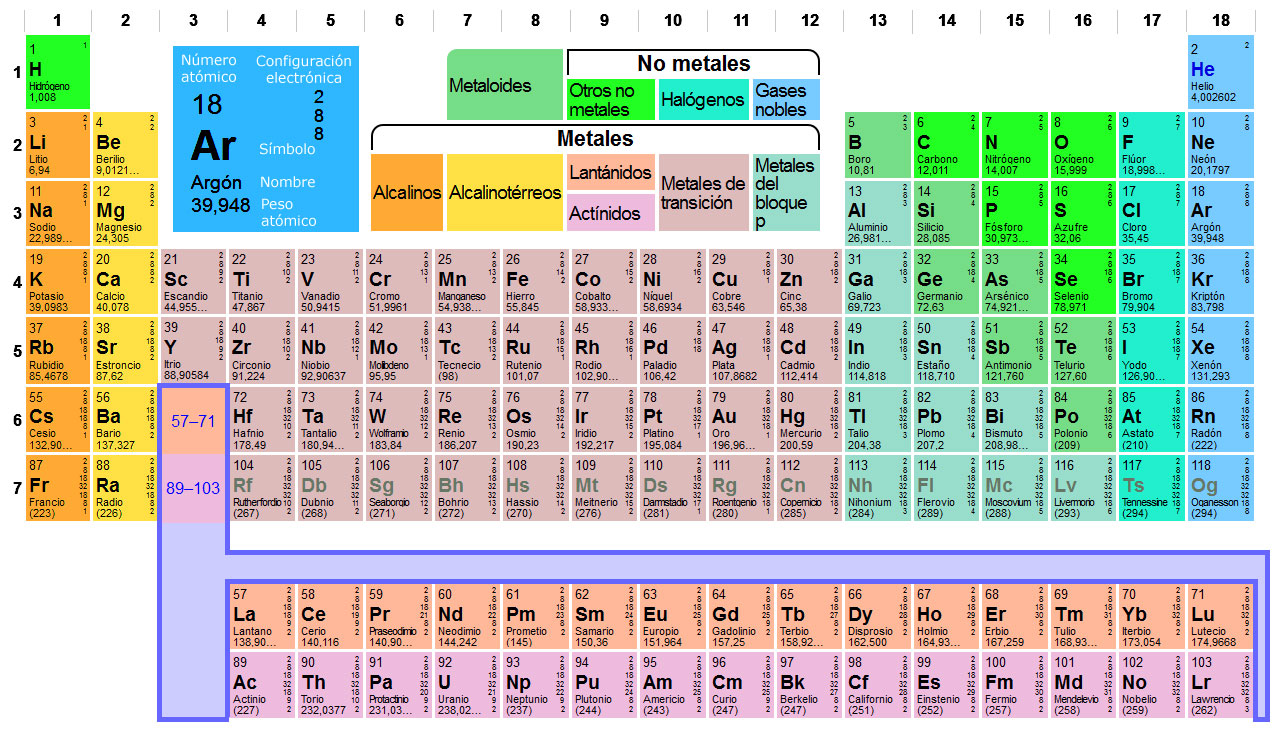
Según la composición de cada átomo se diferencian los distintos
elementos químicos representados en la tabla periódica de los elementos
químicos. En esta tabla podemos encontrar el número atómico y el número másico de cada elemento:
- Número atómico: se representa con la letra Z, indica la cantidad de protones que presenta un átomo, que es igual a la de electrones. Todos los átomos con un mismo número de protones pertenecen al mismo elemento y tienen las mismas propiedades químicas. Por ejemplo todos los átomos con un protón serán de hidrógeno (Z = 1), todos los átomos con dos protones serán de helio (Z = 2).
- Número másico: se representa con la letra A, y hace referencia a la suma de protones y neutrones que contiene el elemento. Los isótopos son dos átomos con el mismo número de protones, pero diferente número de neutrones. Los isótopos de un mismo elemento, tienen unas propiedades químicas y físicas muy parecidas entre sí.
Modelo de Rutherford
Este modelo fue desarrollado por el físico Ernest Rutherford a partir de los resultados obtenidos en lo que hoy se conoce como el experimento de Rutherford
en 1911. Representa un avance sobre el modelo de Thomson, ya que
mantiene que el átomo se compone de una parte positiva y una negativa.
Sin embargo, a diferencia del anterior, postula que la parte positiva se
concentra en un núcleo, el cual también contiene virtualmente toda la
masa del átomo, mientras que los electrones se ubican en una corteza
orbitando al núcleo en órbitas circulares o elípticas con un espacio
vacío entre ellos. A pesar de ser un modelo obsoleto, es la percepción
más común del átomo del público no científico.
Rutherford predijo la existencia del neutrón en el año 1920, por esa razón en el modelo anterior (Thomson), no se habla de este.
Por desgracia, el modelo atómico de Rutherford presentaba varias incongruencias:
- Contradecía las leyes del electromagnetismo de James Clerk Maxwell, las cuales estaban muy comprobadas mediante datos experimentales. Según las leyes de Maxwell, una carga eléctrica en movimiento (en este caso el electrón) debería emitir energía constantemente en forma de radiación y llegaría un momento en que el electrón caería sobre el núcleo y la materia se destruiría. Todo ocurriría muy brevemente.
- No explicaba los espectros atómicos.
Modelo de Bohr
Este modelo es estrictamente un modelo del átomo de hidrógeno tomando como punto de partida el modelo de Rutherford. Niels Bohr trata de incorporar los fenómenos de absorción y emisión de los gases, así como la nueva teoría de la cuantización de la energía desarrollada por Max Planck y el fenómeno del efecto fotoeléctrico observado por Albert Einstein.
«El átomo es un pequeño sistema solar con un núcleo en el centro y
electrones moviéndose alrededor del núcleo en órbitas bien definidas».
Las órbitas están cuantizadas (los e- pueden estar solo en ciertas
órbitas)
- Cada órbita tiene una energía asociada. La más externa es la de mayor energía.
- Los electrones no irradian energía (luz) mientras permanezcan en órbitas estables.
- Los electrones pueden saltar de una a otra órbita. Si lo hace desde una de menor energía a una de mayor energía absorbe un cuanto de energía (una cantidad) igual a la diferencia de energía asociada a cada órbita. Si pasa de una de mayor a una de menor, pierde energía en forma de radiación (luz).
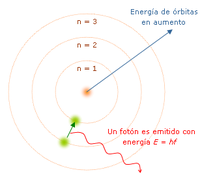
El mayor éxito de Bohr fue dar la explicación al espectro de emisión
del hidrógeno, pero solo la luz de este elemento proporciona una base
para el carácter cuántico de la luz, el fotón es emitido cuando un
electrón cae de una órbita a otra, siendo un pulso de energía radiada.
Bohr no pudo explicar la existencia de órbitas estables y para la condición de cuantización.
Bohr encontró que el momento angular del electrón es h/2π por un método que no puede justificar.
Modelo de Sommerfeld
El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones
de un mismo nivel energético tenían distinta energía, mostrando que
existía un error en el modelo. Su conclusión fue que dentro de un mismo
nivel energético existían subniveles, es decir, energías ligeramente
diferentes. Además desde el punto de vista teórico, Sommerfeld había
encontrado que en ciertos átomos las velocidades de los electrones
alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas.
El físico alemán finalmente Arnold Sommerfeld, con la ayuda de la teoría de la relatividad de Albert Einstein, hizo las siguientes modificaciones del modelo de Bohr:
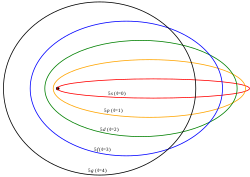
- Los electrones se mueven alrededor del núcleo, en órbitas circulares o elípticas.
- A partir del segundo nivel energético existen dos o más subniveles en el mismo nivel.
- El electrón es una corriente eléctrica minúscula.
En consecuencia, el modelo atómico de Sommerfeld es una
generalización del modelo atómico de Bohr desde el punto de vista
relativista, aunque no pudo demostrar las formas de emisión de las
órbitas elípticas, solo descartó su forma circular.
Modelo de Schrödinger
Después de que Louis-Victor de Broglie propuso la naturaleza ondulatoria de la materia en 1924, la cual fue generalizada por Erwin Schrödinger en 1926, se actualizó nuevamente el modelo del átomo.
En el modelo de Schrödinger se abandona la concepción de los
electrones como esferas diminutas con carga que giran en torno al
núcleo, que es una extrapolación de la experiencia a nivel macroscópico
hacia las diminutas dimensiones del átomo. En vez de esto, Schrödinger
describe a los electrones por medio de una función de onda, el cuadrado de la cual representa la probabilidad de presencia en una región delimitada del espacio. Esta zona de probabilidad se conoce como orbital. La gráfica siguiente muestra los orbitales para los primeros niveles de energía disponibles en el átomo de hidrógeno.
Niveles de energía
Cuando un electrón efectúa una transición entre dos estados
distintos, absorbe o emite un fotón, cuya energía es precisamente la
diferencia entre los dos niveles. La energía de un fotón es proporcional
a su frecuencia, así que cada transición se corresponde con una banda estrecha del espectro electromagnético denominada línea espectral.
Cada elemento químico posee un espectro de líneas característico.
Estas se detectan como líneas de emisión en la radiación de los átomos
del mismo. Por el contrario, si se hace pasar radiación con un espectro
de frecuencias continuo a través de estos, los fotones con la energía
adecuada son absorbidos. Cuando los electrones excitados decaen más
tarde, emiten en direcciones aleatorias, por lo que las frecuencias
características se observan como líneas de absorción oscuras. Las medidas espectroscópicas de la intensidad y anchura de estas líneas permite determinar la composición de una sustancia.
Algunas líneas espectrales se presentan muy juntas entre sí, tanto
que llegaron a confundirse con una sola históricamente, hasta que fue
descubierta su subestructura o estructura fina.
La causa de este fenómeno se encuentra en las diversas correcciones a
considerar en la interacción entre los electrones y el núcleo. Teniendo
en cuenta tan solo la fuerza electrostática, ocurre que algunas de las
configuraciones electrónicas pueden tener la misma energía aun siendo
distintas. El resto de pequeños efectos y fuerzas en el sistema
electrón-núcleo rompe esta redundancia o degeneración, dando lugar a la estructura final. Estos incluyen las correcciones relativistas al movimiento de electrón, la interacción de su momento magnético con el campo eléctrico y con el núcleo.
Interacciones eléctricas entre protones y electrones
Antes del experimento de Rutherford la comunidad científica aceptaba el modelo atómico de Thomson, situación que varió después de la experiencia de Ernest Rutherford.
Los modelos posteriores se basan en una estructura de los átomos con
una masa central cargada positivamente rodeada de una nube de carga
negativa.
Este tipo de estructura del átomo llevó a Rutherford a proponer su
modelo en que los electrones se moverían alrededor del núcleo en
órbitas. Este modelo tiene una dificultad proveniente del hecho de que
una partícula cargada acelerada, como sería necesario para mantenerse en
órbita, radiaría radiación electromagnética, perdiendo energía. Las leyes de Newton, junto con las ecuaciones de Maxwell del electromagnetismo aplicadas al átomo de Rutherford llevan a que en un tiempo del orden de 10 s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.
¿Todavia no estas registrado?
¡Unete a Cerebriti! Podras crear juegos, sumar puntos y competir con tus amigos para demostrar quien es el que mas sabe
O
Registrate con el mail 

Das tu consentimiento para que tus datos personales sean transferidos y procesados por Cerebriti
¿Ya tienes cuenta en Cerebriti?
Crear canal
Iniciar sesión Cerebriti
O
¿Olvidaste tu contraseña?
Para recuperar tu contraseña, introduce tu dirección de email y te enviaremos instrucciones sobre cómo crear una nueva contraseña.
Contacta con Cerebriti
¿Te interesaría publicitarte en nuestra página? Déjanos tus datos y nos pondremos en contacto contigo
Has elegido retar a Carlos.
Para comenzar este reto de mentes priviligedias, elige el tipo de reto:
¿A quién quieres retar?
Busca a tu contrincante entre los jugadores de Cerebriti:
Reto aleatorio
Se elegirá un juego al azar dentro de la categoría que elijas:
Reto a un juego concreto
Encuentra el juego al que quieres retar a tu oponente en nuestro buscador:
Lanzar reto 

¿Cómo funcionan los retos?









Comentarios
Publicar un comentario